Автор:
Randy Alexander
Дата создания:
2 Апрель 2021
Дата обновления:
1 Июль 2024

Содержание
Химическое уравнение - это символическое представление химической реакции. Реагенты написаны слева, а продукт - справа. Закон сохранения массы указывает на то, что в химической реакции атомы не рождаются и не теряются, поэтому количество атомов, присутствующих в реагенте, должно быть равно количеству атомов, присутствующих в реакции. товар. Следуя этому руководству, вы можете по-разному сбалансировать химические уравнения.
Шаги
Метод 1 из 2: балансировка традиционным методом.
Напишите данное уравнение. В этом примере у вас будет: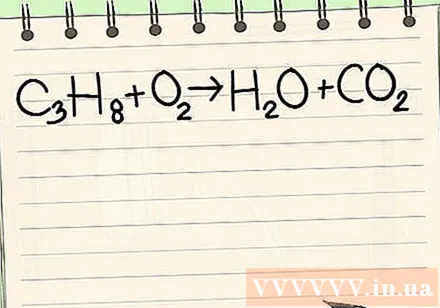
- C3ЧАС8 + O2 -> H2O + CO2
- Эта реакция происходит, когда пропан (C3ЧАС8сгорел в кислороде с образованием воды и углекислого газа.

Запишите количество атомов для каждого элемента, который есть на каждой стороне уравнения. См. Индексы ниже рядом с каждым атомом, чтобы найти количество атомов в уравнении.- Слева: 3 углерода, 8 водорода и 2 кислорода.
- Справа: 1 атом углерода, 2 атома водорода и 3 атома кислорода.
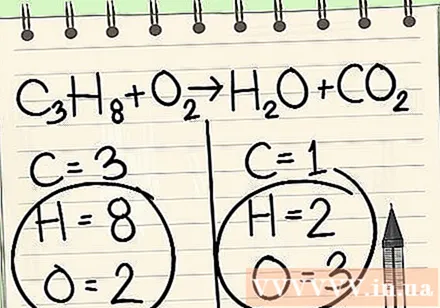
В конце концов, всегда оставляйте водород и кислород.
Если у вас осталось более одного элемента для балансировки: Выберите элемент, который присутствует только в одной молекуле реагента и только в одной молекуле продукта. Это означает, что вам нужно сначала сбалансировать атомы углерода.
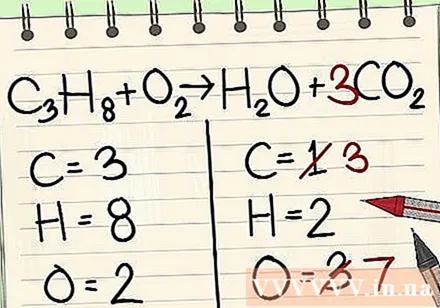
Добавьте коэффициент для отдельных атомов углерода в правую часть уравнения, чтобы сбалансировать его с тремя атомами углерода в левой части уравнения.- C3ЧАС8 + O2 -> H2O + 3CO2
- Коэффициент 3 перед углеродом с правой стороны означает, что имеется 3 атома углерода, а третий показатель слева указывает на 3 атома углерода.
- В химическом уравнении вы можете изменить коэффициент, но не индекс.
Далее идет атомный баланс водорода. Слева у вас 8 атомов водорода. Следовательно, вам понадобится 8 с правой стороны.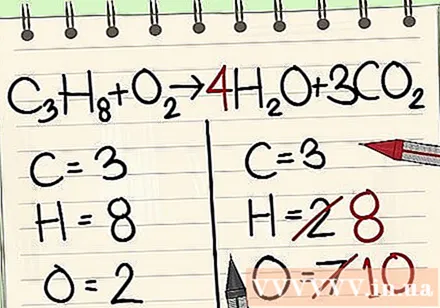
- C3ЧАС8 + O2 -> 4H2O + 3CO2
- Справа от часа вы добавляете 4 как множитель, потому что нижнее число показывает, что у вас уже есть 2 атома водорода.
- Если умножить 4 на 2, получится 8.
- Остальные 6 атомов кислорода принадлежат 3CO2. (3x2 = 6 атомов кислорода + 4 других атома кислорода = 10)
Сбалансируйте атомы кислорода.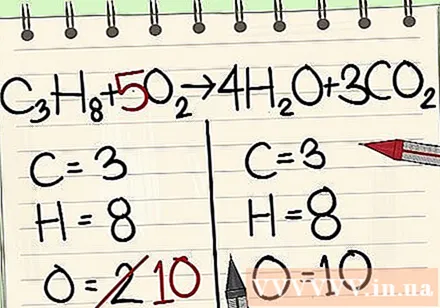
- Поскольку вы добавили коэффициенты к молекулам справа от уравнения, количество атомов кислорода изменилось. Теперь у вас есть 4 атома кислорода в молекуле воды и 6 атомов кислорода в молекуле углекислого газа. Всего у нас 10 атомов кислорода.
- Добавьте коэффициент 5 к молекуле кислорода слева от уравнения. Теперь у вас по 10 молекул кислорода с каждой стороны.
- C3ЧАС8 + 5O2 -> 4H2O + 3CO2.

- Атомы углерода, водорода и кислорода находятся в равновесии. Ваше уравнение завершено.
Метод 2 из 2: балансировка по алгебраическому методу
Напишите уравнения в соответствии с символами и формулами. Пример a = 1 и напишите уравнение на основе этой формулы.
Замените цифры их переменными.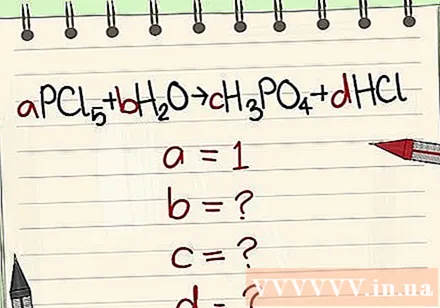
Проверьте количество элементов на стороне реакции, а также на стороне продукта.
- Пример: aPCl5 + bH2O = cH3PO4 + dHCl, так что a = 1 b = c = d = и разделяя элементы P, Cl, H, O, так что вы получаете a = 1 b = 4 c = 1 d = 5 .
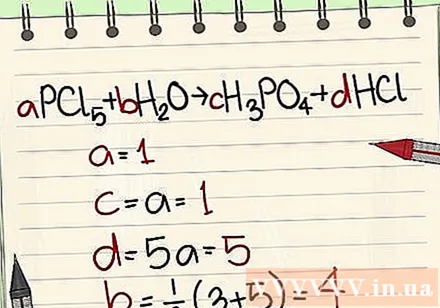
- Пример: aPCl5 + bH2O = cH3PO4 + dHCl, так что a = 1 b = c = d = и разделяя элементы P, Cl, H, O, так что вы получаете a = 1 b = 4 c = 1 d = 5 .
Совет
- Не забудьте упростить уравнение.
- Если у вас возникли проблемы, вы можете ввести уравнение в онлайн-балансировщик, чтобы сбалансировать его. Помните, что когда вы сдаете экзамен, у вас нет доступа к онлайн-балансу, поэтому не полагайтесь на него.
Предупреждение
- Никогда не используйте коэффициент как дробь в химическом уравнении - вы не можете разделить молекулы или атомы в химической реакции.
- В процессе равновесия вы можете использовать дроби, но уравнение не будет сбалансировано, если коэффициенты по-прежнему являются дробями.
- Чтобы удалить дроби, умножьте все уравнение (левое и правое) на знаменатель дроби.